Merkaptaan
'n Merkaptaan is 'n organiese verbinding met die funksionele groep R-SH, waar R 'n alkiel of 'n ander organiese komponent voorstel.[1][2] Die Engelse term "Mercaptan" (mərˈkæptæn)[3] is in 1832 deur William Christopher Zeise bekendgestel en is afgelei van die Latynse mercurium captāns (in Engels: "capturing mercury"), of "vaslegging van kwik", omdat die tiolaatgroep (RS−) baie sterk bind met kwikverbindings.[4]
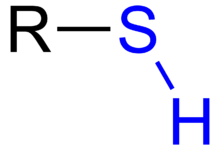
Dit word ook 'n tiol genoem, what 'n kombinasie van "tio-" (wat van Grieks θεῖον (teion) afkomstig is en "swael" beteken) en "alkohol".[5] Die –SH funksionele groep self word óf 'n tiolgroep óf 'n sulfhidrielgroep genoem.
Baie merkaptane het sterk reuke soos die van knoffel of vrot eiers. Merkaptane word as reukmiddels gebruik om 'n aardgaslekkasie (die gas in suiwer vorm is reukloos) op te spoor, en die "reuk van aardgas" is te danke aan die reuk van die merkaptaan wat as reukmiddel gebruik word.
Kookpunte en oplosbaarheid
wysigMerkaptane toon min assosiasie deur waterstofbinding, beide met watermolekules en onder mekaar. Hulle het dus laer kookpunte en is minder oplosbaar in water en ander polêre oplosmiddels as alkohole met 'n soortgelyke molekulêre gewig. Om hierdie rede het tiole en ooreenstemmende tioeter funksionele groepisomere ook soortgelyke oplosbaarheidseienskappe en kookpunte, terwyl dieselfde nie waar is van alkohole en hul ooreenstemmende isomeriese eters nie.
Verbindings
wysigDie S-H-binding in merkaptane is swak in vergelyking met die O-H-binding in alkohole. Vir CH3X−H is die bindingsentalpieë 365,07 ± 2,1 kcal/mol vir X=S en 440,2 ± 3,0 kcal/mol vir X=O.[6]
Suur
wysigMerkaptane kan maklik gedeprotoneer word.[7] In vergelyke met die alkohole is merkaptane meer suur. Die gekonjugeerde basis van 'n tiol (of merkaptaan) word 'n tiolaat (of merkaptanaat) genoem. Butaantiol het 'n pKa van 10,5 teenoor 15 vir butanol. Tiofenol het 'n pKa van 6, teenoor 10 vir fenol. 'n Hoogs suur tiol is pentafluorotiofenol (C6F5SH) met 'n pKa van 2,68. Dus kan tiolate uit tiols verkry word deur behandeling met alkalimetaalhidroksiede.
Verwysings
wysig- ↑ Patai, Saul, red. (1974). The chemistry of the thiol group (in Engels). London: Wiley. ISBN 978-0-471-66949-4.
- ↑ R. J. Cremlyn (1996). An Introduction to Organosulfur Chemistry (in Engels). Chichester: John Wiley and Sons. ISBN 978-0-471-95512-2.
- ↑ "Definisie van "mercaptan"". Dictionary.com (in Engels). 13 November 2012. Geargiveer vanaf die oorspronklike op 5 Maart 2016. Besoek op 31 Desember 2019.
- ↑ Zeise, William Christopher (1834). "Sur le mercaptan; avec des observations sur d'autres produits resultant de l'action des sulfovinates ainsi que de l'huile de vin, sur des sulfures metalliques" [Op mercaptan; met waarnemings oor ander produkte wat voortspruit uit die werking van sulfovinate [tipies etielwaterstofsulfaat] sowel as olie van wyn ['n mengsel van diethylsulfaat en etileen polimere] op metaal sulfiede]. Annales de Chimie et de Physique (in Frans). 56: 87–97. Geargiveer vanaf die oorspronklike op 20 Maart 2015.
- ↑ "Henry George Liddell, Robert Scott, A Greek-English Lexicon, θεῖον". Perseus Digital Library (in Engels en Grieks). 10 Mei 2017. Geargiveer vanaf die oorspronklike op 6 Januarie 2020. Besoek op 31 Desember 2019.
{{cite web}}: AS1-onderhoud: onerkende taal (link) - ↑ Luo, Y.-R.; Cheng, J.-P. (2017). "Bond Dissociation Energies". In J. R. Rumble (red.). Handbook of Chemistry and Physics (in Engels). CRC Press.
{{cite book}}: AS1-onderhoud: gebruik authors-parameter (link) - ↑ M. E. Alonso and H. Aragona (1978). "Sulfide Synthesis in Preparation of Unsymmetrical Dialkyl Disulfides: Sec-butyl Isopropyl Disulfide". Org. Synth. (in Engels). 58: 147. doi:10.15227/orgsyn.058.0147.
{{cite journal}}: AS1-onderhoud: gebruik authors-parameter (link)