Glisien
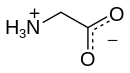
Glisien (afgekort as Gly of G) is die aminosuur wat 'n enkele waterstof atoom as syketting het. Dit is die eenvoudigste moontlike aminosuur. Die chemiese formule van glisien is NH2‐CH2‐COOH. Glisien is een van die proteïnogeniese aminosure. In die genetiese kode, kodeer alle kodons wat met GG begin, naamlik GGU, GGC, GGA, en GGG, vir glisien.
|
Algemeen | |
|---|---|
| Naam | Glisien |
| IUSTC-naam | Aminoetanoësuur |
 |
 |
| Chemiese formule | C2H5O2N1 |
| Molêre massa | 75.07 g/mol |
| CAS-nommer | 56-40-6 |
| Voorkoms | wit vaste stof |
| Fasegedrag | |
| Smeltpunt | 233 °C (dekomposisie) |
| Kookpunt | |
| Digtheid | 1.607 g/cm3 |
| Oplosbaarheid | |
|
Suur-basis eienskappe | |
| pKa | |
|
Veiligheid | |
| Flitspunt | |
| LD50 | 2600 mg/kg (muis, oraal) |
|
Tensy anders vermeld is alle data vir standaardtemperatuur en -druk toestande. | |
| Portaal | |
Glisien is 'n kleurlose kristallyne vaste stof met 'n soet smaak. Dit is die enigste achirale proteïnogeniese aminosuur. Dit kan inpas in hidrofiliese of hidrofobiese omgewings, as gevolg van sy minimale syketting van slegs een waterstofatoom. Die asielradikaal is glisiel.

Geskiedenis en etimologie
wysigGlisien is in 1820 deur Henri Braconnot ontdek toe hy gelatien gehidroliseer het deur dit met swaelsuur te kook.[1] Hy het dit oorspronklik "suiker van gelatien" genoem,[2] maar 'n student van Liebig het getoon dat dit Stikstof bevat, en Berzelius het dit "glisien" herdoop.[3] Die naam is afkomstig van die antieke griekse woord γλυκύς ("soet")[4] (wat ook verband hou met die voorvoegsels gliko- en gluko-, soos in glikoproteïne en glukose). 'n Ander vroeë naam vir glisien was "glycocoll".[5]
Produksie
wysigHoewel glisien uit gehidroliseerde proteïen geïsoleer kan word, word hierdie metode nie gebruik vir industriële produksie nie, want dit kan meer gerieflik deur chemiese sintese vervaardig word.[6] Die twee belangrikste prosesse is aminering van chloroasynsuur met ammoniak, wat glisien en ammonium chloried as produkte lewer,[7] en die Strecker aminosuursintese,[8] wat die belangrikste sintetiese metode is in die Verenigde State en Japan.[9] Ongeveer 15 duisend ton word jaarliks op hierdie manier geproduseer.[10]
Glisien is ook 'n neweproduk in die sintese van EDTA, wat voortspruit uit die reaksies van die ammoniak koproduk.[11]
Suur-basis-eienskappe
wysigIn waterige oplossing is glisien self amfoteries: by lae pH kan die molekule met 'n pKa van ongeveer 2.4 geprotoneer word, en teen 'n hoë pH verloor dit 'n proton met 'n pKa van ongeveer 9.6 - die presiese waardes van die pKa hang af van die temperatuur en ioniese sterkte van die oplossing.
Metabolisme
wysigBiosintese
wysigGlisien is nie noodsaaklik in die menslike dieet nie, aangesien dit in die liggaam uit die aminosuur serien gesintetiseer kan word, wat op sy beurt van 3-fosfogliseraat gevorm word, maar die metaboliese kapasiteit vir glisien biosintese nie voldoen aan die behoefte vir kollageen sintese nie.[12] In die meeste organismes, kataliseer die ensiem serien hidroksimetieltransferase hierdie transformasie via die kofaktor piridoksaal fosfaat:
- serien + tetrahidrofolaat → glisien + N5,N10-Metileentetrahidrofolaat + H2O
In die lewer van werweldiere, word glisiensintese gekataliseer deur glisien sintase (ook genoem glisien klowingsensiem). Hierdie reaksie is maklik omkeerbaar:
- CO2 + NH+
4 + N5,N10-Metileentetrahidrofolaat + NADH + H+ ⇌ Glisien + tetrahidrofolaat + NAD+
Afbraak
wysigGlisien word volgens drie reaksiepaaie afgebreek. Die oorheersende pad in diere en plante is die omgekeerde van die glisiensintase pad hierbo. In hierdie konteks, word die ensiemstelsel gewoonlik die glisien klowingstelsel genoem:
- Glisien + tetrahidrofolaat + NAD+ ⇌ CO2 + NH+
4 + N5,N10-Metileentetrahidrofolaat + NADH + H+
Volgens die tweede pad, word glisien in twee stappe afgebreek. Die eerste stap is die omgekeerde van glisienbiosintese vanaf serien met serien hidroksimetieltransferase. Serien word dan omgeskakel na piruvaat deur serien dehidratase.
In die derde pad van glisienafbraak, word glisien omgeskakel na glioksilaat deur D-aminosuur oksidase. Glioksilaat word dan deur hepatiese laktaat dehidrogenase na oksalaat geoksideer in 'n NAD+-afhanklike reaksie.
Die half-lewe van glisien en sy uitskakeling uit die liggaam wissel aansienlik afhanklik van dosis. In een studie, het die half-lewe tussen 0.5 en 4.0 ure gewissel.[13]
Fisiologiese funksie
wysigDie belangrikste funksie van glisien is as 'n voorloper vir proteïene. Die meeste proteïene bevat slegs klein hoeveelhede van glisien, maar kollageen is 'n noemenswaardige uitsondering: dit bevat sowat 35% glisien as gevolg van sy herhalende rol in die vorming van kollageen se heliksstruktuur in samewerking met hidroksiprolien.[14][15] In die genetiese kode, word glisien gekodeer deur alle kodons wat begin met GG, naamlik GGU, GGC, GGA en GGG.
As 'n biosintetiese tussenproduk
wysigIn hoër eukariote, word δ-aminolevuliniese suur, die belangrikste voorloper tot porfiriene, uit glisien en suksiniel-CoA deur die ensiem ALA sintase gesintetiseer. Glisien lewer die sentrale C2N subeenheid van alle puriene.
As'n neurotransmitter
wysigGlisien is 'n inhiberende neurotransmitter in die sentrale senuweestelsel, veral in die rugmurg, breinstam, en retina. Wanneer glisienreseptore geaktiveer word, vloei chloriedione deur ionotropiese reseptore in die neuron in, wat 'n Inhiberende postsinaptiese potensiaal (IPSP) veroorsaak. Strignien is 'n sterk antagonis van ionotropiese glisienreseptore, terwyl bicucullien is 'n swak antagonis is. Glisien is 'n vereiste mede-agonis saam met glutamaat vir NMDA reseptore. In teenstelling met die inhiberende rol van glisien in die rugmurg, word hierdie gedrag op die (NMDA) glutamatergiese reseptore gefasiliteer, wat prikkelend inwerk.[16] Die LD50 van glisien is 7930 mg/kg in rotte (mondeling),[17] en dit veroorsaak gewoonlik die dood deur hiperprikkelbaarheid.
Gebruik
wysigIn die VSA, word glisien gewoonlik in twee grade verkoop: VSA Farmakopee ("USP"), en tegniese graad. USP graad verkope maak ongeveer 80% tot 85% van die Amerikaanse mark vir glisien uit. Waar die kliënt se suiwerder glisien benodig as wat onder die USP standaard voorgeskryf word, byvoorbeeld vir farmaseutiese toepassings soos binneaarse inspuitings, word farmaseutiese graad glisien, dikwels met eie spesifikasies teen 'n hoër prys as USP graad glisien, gebruik. Tegniese graad glisien, wat nie noodwendig aan USP standaarde voldoen nie, word teen 'n laer prys verskaf vir gebruik in industriële toepassings; bv. as 'n metaalkompleksering en afwerkingsdoeleindes.[18]
Mens- en diervoedsel
wysigUSP glisien het 'n wye verskeidenheid van gebruike, insluitend as 'n bymiddel in troeteldier kos en voer, in voedsel en farmaseutiese produkte as 'n versoeter of smaak intensifiseerder, of as 'n komponent van voedselaanvullings en proteïendrankies. Sekere farmaseutiese formulerings sluit glisien in om gastriese opname van die aktiewe bestanddele te verbeter.
Skoonheidsmiddels en diverse toepassings
wysigGlisien dien as 'n buffer in teensuurmiddels, pynstillers, sweetweerders, skoonheidsmiddels en toiletware.
'n Verskeidenheid van industriële en chemiese prosesse gebruik glisien of sy afgeleides, soos in die produksie van kunsmis en metaalkomplekserende chemikalië.[19]
Chemiese grondstof
wysigGlisien is 'n tussenproduk in die sintese van 'n verskeidenheid van chemiese produkte. Dit word gebruik in die vervaardiging van die onkruiddoder glifosaat.[20]
Laboratorium navorsing
wysigGlisien is 'n belangrike komponent van verskeie oplossings wat gebruik word in die poliakrilamied elektroforese van proteïene. Dit dien as 'n buffer, om pH te handhaaf, en om van skade aan die monster tydens elektroforese te voorkom. Glisien word ook gebruik om proteïen-etiketterende teenliggaampies van die Western-klad membrane te stroop om die sondering van verskeie proteïene wat deur die SDS-PAGE-gel geskei is, moontlik te maak. Dit maak dit moontlik om meer data uit die dieselfde monster te verkry, met hoër betroubaarheid, verminder die benodigde monsterverwerking, en maak dat minder monsters benodig word.
Teenwoordigheid in die ruimte
wysigDie teenwoordigheid van glisien buite die aarde is bevestig in 2009, gebaseer op die ontleding van monsters van komeet Wild 2 wat geneem is in 2004 deur die NASA - ruimtetuig Stardust en daarna teruggebring is aarde toe. Glisien is voorheen geïdentifiseer in die Murchison meteoriet in 1970.[21] Die ontdekking van glisien in komete versterk die teorie van panspermia, wat beweer dat die "boublokke" van die lewe wydverspreid oor die heelal vookom.[22] In 2016, is die opsporing van glisien binne Komeet 67P/Churyumov-Gerasimenko deur die Rosetta-ruimtetuig aangekondig.[23]
Die opsporing van glisien buite die sonnestelsel in die interstellêre medium is 'n onderwerp van wetenskaplike debat.[24] In 2008 het die Max Planck-Instituut vir Radio-Astronomie die glisienagtige molekuul aminoasetonitriel in die Groot Molekuul Heimat, 'n reuse-gas wolk naby die galaktiese middelpunt in die Boogskutter sterrebeeld, opgespoor.[25]
Verwysings
wysig- ↑ R.H.A. Plimmer (1912) [1908]. R.H.A. Plimmer; F.G. Hopkins (reds.). The chemical composition of the proteins. Monographs on biochemistry. Vol. Part I. Analysis (2nd uitg.). London: Longmans, Green and Co. p. 82. Besoek op 18 Januarie 2010.
- ↑ MacKenzie, Colin (1822). One Thousand Experiments in Chemistry: With Illustrations of Natural Phenomena; and Practical Observations on the Manufacturing and Chemical Processes at Present Pursued in the Successful Cultivation of the Useful Arts ... (in Engels). Sir R. Phillips and Company.
- ↑ Nye, Mary Jo (1999). Before Big Science: The Pursuit of Modern Chemistry and Physics, 1800-1940 (in Engels). Harvard University Press. ISBN 9780674063822.
- ↑ "glycine". Oxford Dictionaries. Geargiveer vanaf die oorspronklike op 15 September 2016. Besoek op 6 Desember 2015.
- ↑ Ihde, Aaron J. (1970). The Development of Modern Chemistry (in Engels). Courier Corporation. ISBN 9780486642352.
- ↑ Okafor, Nduka (9 Maart 2016). Modern Industrial Microbiology and Biotechnology (in Engels). CRC Press. ISBN 9781439843239.
- ↑ Ingersoll, A. W.; Babcock, S. H. (1932). "Hippuric acid". Org. Synth. 12: 40.; Coll. Vol., 2, p. 328
- ↑ Wiley (14 Desember 2007). Kirk-Othmer Food and Feed Technology, 2 Volume Set (in Engels). John Wiley & Sons. ISBN 9780470174487.
- ↑ "Glycine Conference (prelim)". USITC. Geargiveer vanaf die oorspronklike op 22 Februarie 2012. Besoek op 13 Junie 2014.
{{cite web}}: CS1 maint: bot: original URL status unknown (link) - ↑ Drauz, Karlheinz; Grayson, Ian; Kleemann, Axel; Krimmer, Hans-Peter; Leuchtenberger, Wolfgang and Weckbecker, Christoph (2007) "Amino Acids" in Ullmann's Encyclopedia of Industrial Chemistry, Wiley-VCH, Weinheim. doi:10.1002/14356007.a02_057.pub2
- ↑ Hart, J. Roger (2005) "Ethylenediaminetetraacetic Acid and Related Chelating Agents" in Ullmann's Encyclopedia of Industrial Chemistry, Wiley-VCH, Weinheim. doi:10.1002/14356007.a10_095
- ↑ Meléndez-Hevia, E; De Paz-Lugo, P; Cornish-Bowden, A; Cárdenas, M. L. (Desember 2009). "A weak link in metabolism: the metabolic capacity for glycine biosynthesis does not satisfy the need for collagen synthesis". Journal of biosciences. 34 (6): 853–72. doi:10.1007/s12038-009-0100-9. PMID 20093739.
- ↑ Hahn RG (1993). "Dose-dependent half-life of glycine". Urological Research. 21 (4): 289–291. doi:10.1007/BF00307714. PMID 8212419.
- ↑ Nelson, David L.; Cox, Michael M. (2005), Principles of Biochemistry (4th ed.), New York: W. H. Freeman, pp. 127, 675–77, 844, 854, ISBN 0-7167-4339-6
- ↑ Szpak, Paul (2011). "Fish bone chemistry and ultrastructure: implications for taphonomy and stable isotope analysis". Journal of Archaeological Science. 38 (12): 3358–3372. doi:10.1016/j.jas.2011.07.022.
- ↑ "Recent development in NMDA receptors". Chinese Medical Journal. 2000.
- ↑ "Safety (MSDS) data for glycine" (in Engels). The Physical and Theoretical Chemistry Laboratory Oxford University. 2005. Geargiveer vanaf die oorspronklike op 20 Oktober 2007. Besoek op 1 November 2006.
- ↑ "Glycine From Japan and Korea" (PDF). U.S. International Trade Commission. Januarie 2008. Besoek op 13 Junie 2014.
- ↑ "Notice of Preliminary Determination of Sales at Less Than Fair Value: Glycine From India" Federal Register 72 (7 November 2007): 62827.
- ↑ Stahl, Shannon S.; Alsters, Paul L. (13 Julie 2016). Liquid Phase Aerobic Oxidation Catalysis: Industrial Applications and Academic Perspectives (in Engels). John Wiley & Sons. ISBN 9783527690152.
- ↑ Kvenvolden, Keith A.; Lawless, James; Pering, Katherine; Peterson, Etta; Flores, Jose; Ponnamperuma, Cyril; Kaplan, Isaac R.; Moore, Carleton (1970). "Evidence for extraterrestrial amino-acids and hydrocarbons in the Murchison meteorite". Nature. 228 (5275): 923–926. Bibcode:1970Natur.228..923K. doi:10.1038/228923a0. PMID 5482102.
- ↑ Reuters (18 Augustus 2009). "Building block of life found on comet - Thomson Reuters 2009" (in Engels). Geargiveer vanaf die oorspronklike op 18 September 2009. Besoek op 18 Augustus 2009.
{{cite news}}:|author=has generic name (hulp) - ↑ European Space Agency (27 Mei 2016). "Rosetta's comet contains ingredients for life" (in Engels). Geargiveer vanaf die oorspronklike op 1 Maart 2019. Besoek op 5 Junie 2016.
- ↑ Snyder LE, Lovas FJ, Hollis JM, et al. (2005). "A rigorous attempt to verify interstellar glycine". Astrophys J. 619 (2): 914–930. arXiv:astro-ph/0410335. Bibcode:2005ApJ...619..914S. doi:10.1086/426677.
- ↑ Staff. "Organic Molecule, Amino Acid-Like, Found In Constellation Sagittarius 27 March 2008 - Science Daily". Besoek op 16 September 2008.
Verdere leesstof
wysig- "Interstellar glycine". Astrophys J. 593 (2): 848–867. 2003. doi:10.1086/375637.
- Rachel Nowak. "Amino acid found in deep space - 18 July 2002 - New Scientist"
Eksterne skakels
wysig- Glycine MS Spectrum
- Glycine at PDRHealth.com
- Glycine cleavage system
- Glycine Therapy - A New Direction for Schizophrenia Treatment?
- "Organic Molecule, Amino Acid-Like, Found In Constellation Sagittarius". ScienceDaily. 27 Maart 2008.
- Guochuan E. Tsai (1 Desember 2008). "A New Class of Antipsychotic Drugs: Enhancing Neurotransmission Mediated by NMDA Receptors". Psychiatric Times. 25 (14). Geargiveer vanaf die oorspronklike op 3 Oktober 2012. Besoek op 4 Oktober 2017.
- ChemSub Online (Glycine).
- NASA scientists have discovered glycine, a fundamental building block of life, in samples of comet Wild 2 returned by NASA's Stardust spacecraft.